1. La cinetica chimica e la catalisi sono state spiegate nel corso di Chimica e Propedeutica Biochimica; e' molto consigliabile rileggere la spiegazione pertinente al link qui fornito. 2. Gli enzimi sono catalizzatori biologici molto specifici. Gli enzimi sono proteine capaci di catalizzare reazioni chimiche di interesse per il metabolismo. Sono molto specifici: ogni enzima catalizza una sola reazione chimica su un solo reagente o su pochi reagenti tra loro simili. Il reagente delle reazioni catalizzate da enzimi prende il nome di substrato dell'enzima. Le reazioni biochimiche, alla temperatura corporea sono estremamente lente; in pratica si puo' affermare che in assenza dell'enzima non avverrebbero affatto. L'enzima, combinandosi in modo transitorio con il reagente della reazione, fornisce un meccanismo di reazione che ha energia di attivazione piu' bassa di quella della reazione non catalizzata: 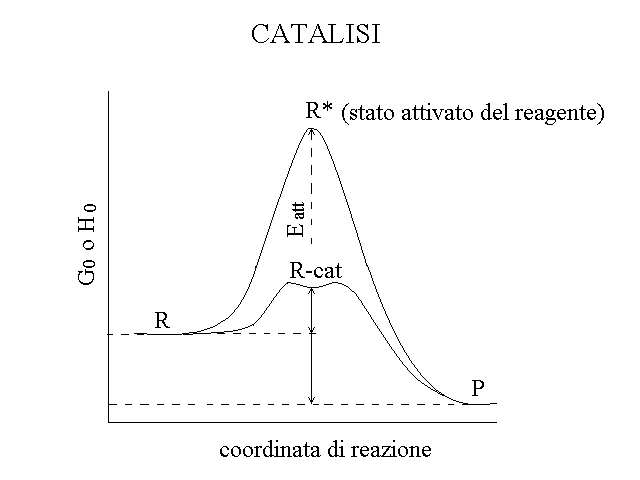 3. Enzimi ad un solo substrato. Sono i piu' semplici da studiare e descrivere, ma costituiscono una minoranza (la maggioranza degli enzimi catalizza reazioni che richiedono due substrati). Esempi di questo tipo di enzimi sono le isomerasi e le idrolasi. Esempi di reazioni di questo tipo sono: maltosio + H2O --> 2 glucosio (enzima: maltasi) 4. E' interessante confrontare l'andamento temporale della reazione e la dipendenza della sua velocita' dalla concentrazione di substrato in presenza ed in assenza dell'enzima: 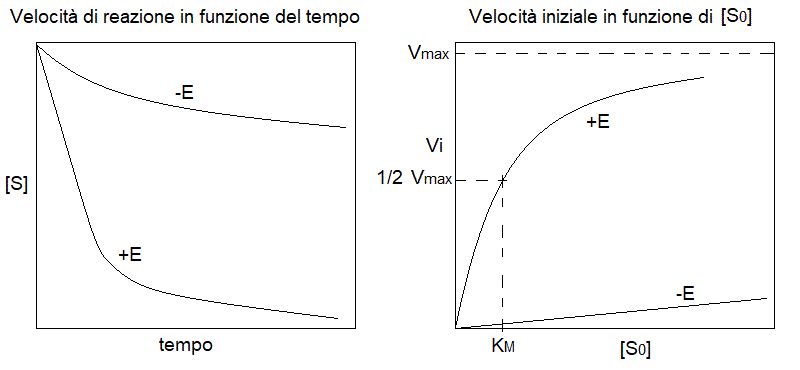 5. La dipendenza iperbolica, che ricorda l'equilibrio chimico invece della cinetica fu spiegata da Michaelis e Menten ricorrendo all'ipotesi che l'enzima formi un complesso instabile con il substrato (complesso di Michaelis). Il modello di Michaelis e Menten e' stato spiegato nel Corso di Chimica e Propedeutica Biochimica. L'equazione di Michelis e Menten (vedi sotto) e' valida soltanto per le condizioni di stato stazionario, nelle quali le concentrazioni delle diverse specie chimiche dell'enzima (E ed ES) sono (approssimativamente) costanti. 6. L'iperbole di Michaelis e Menten puo' essere linearizzata nel grafico dei doppi reciproci, di Lineweaver e Burk. In origine il motivo di questa trasformazione era quello di facilitare l'analisi in un epoca nella quale i computers non erano disponibili; ma la rappresentazione e' entrata nell'uso ed e' tuttora utilizzata anche se introduce distorsioni nella rappresentazione dell'errore sperimentale. la trasformazione e' la seguente: Lineweaver e Burk: 1/V = 1 / Vmax + KM / Vmax [S] 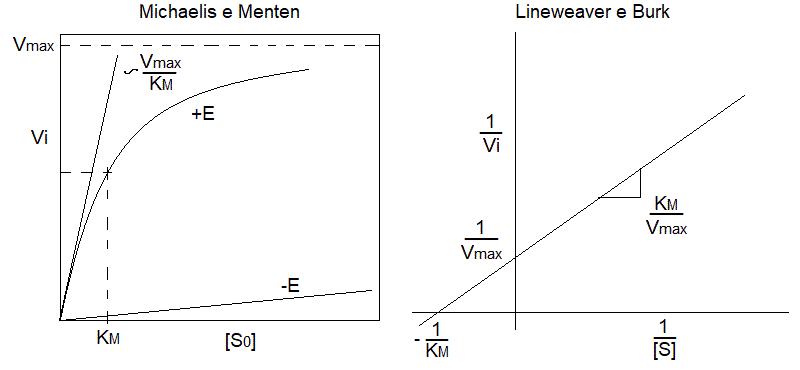 7. Un esempio di meccanismo catalitico: le proteasi a serina. Dal punto di vista del meccanismo di reazione, ogni enzima e' un caso a se; ciononostante e' importante avere in mente almeno un esempio di un meccanismo di reazione. Uno dei casi meglio studiati e' quello delle proteasi a serina come tripsina, chimotripsina, etc. che idrolizzano i legami peptidici interni alle molecole proteiche nel corso dei processi digestivi. 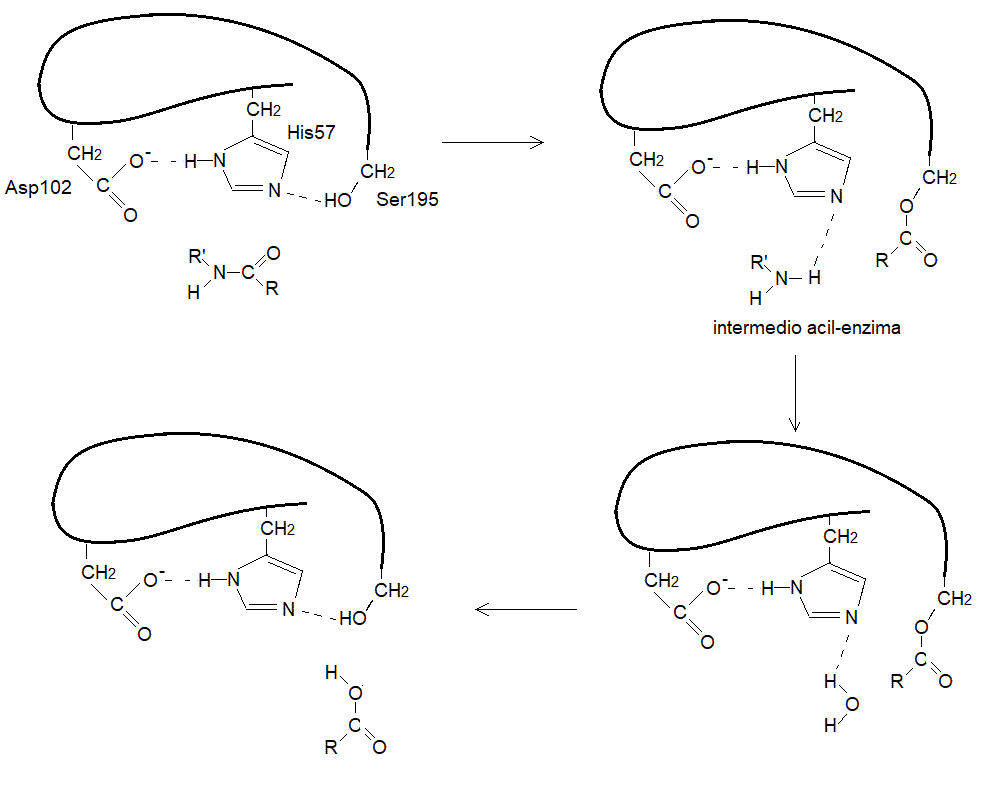 8. Effetto del pH. Nel meccanismo di molti enzimi intervengono eventi di catalisi acido-base (estrazione o donazione di ioni idrogeno). In questi casi per la catalisi sono essenziali residui aminoacidici dissociabili (nell'esempio delle proteasi a serina His 57 e Asp 102). Se lo stato di protonazione di questi residui viene alterato cambiando il pH della soluzione, la catalisi diventa meno efficiente e soltanto la frazione di enzima che si trova negli stati di protonazione "giusti" risulta attivo. Pertanto l'attività di quasi tutti gli enzimi presenta una dipendenza dal pH con un valore ottimale prossimo a quello presente nell'ambiente in cui l'enzima deve svolgere la sua funzione fisiologica; al di sopra o al di sotto di questo valore in genere l'attivita' dell'enzima diminuisce fino ad annullarsi. Ad esempio la tripsina presenta un pH ottimale di 7.2-7.6.  9. Catalisi enzimatica di reazioni reversibili. Quando la reazione chimica catalizzata dall'enzima e' reversibile, come accade di frequente (si pensi al caso delle isomerasi che convertono tra loro due isomeri), l'enzima accelera il raggiungimento della condizione di equilibrio, ma non cambia il valore della costante. Questo implica che la reazione procede sempre nella direzione indicata dalla sua costante di equilibrio; se l'organismo ha bisogno di mandarla nella direzione opposta, deve utilizzare meccanismi specifici, ad es. accoppiamento con idrolisi di ATP, o con ossidazione di NADH; oppure deve rimuovere il prodotto di reazione con un'altra trasformazione, piu' vantaggiosa, e mantenere la concentrazione del prodotto al di sotto del suo valore di equilibrio. Questo accade ad esempio nella glicolisi per la trasformazione di P-enolpiruvato in enolpiruvato (energeticamente svantaggiosa) seguita dalla trasformazione di enolpiruvato in piruvato (vantaggiosa). 
10. Inibizione. Ogni cellula possiede un nutrito corredo enzimatico, e alcuni enzimi vengono secreti per agire nell'ambiente extracellulare. Puo' accadere che l'attivita' degli enzimi presenti in un certo distretto risulti in certi momenti non necessaria o addirittura dannosa, sebbene sia utile che l'enzima rimanga disponibile per poter essere rapidamente utilizzato nel momento in cui risultasse necessario. Un esempio di questa condizione e' dato dagli enzimi della coagulazione: devono essere costantemente presenti nel sangue per poter intervenire istantaneamente in caso di emorragia, ma non devono essere attivi finche' l'emorragia non si verifica. La soluzione a questo problema e' l'inibizione enzimatica: la presenza di una piccola molecola capace di formare un complesso reversibile con l'enzima e di bloccarne temporaneamente l'attivita'. Esistono due tipi fondamentali di inibizione enzimatica: competitiva e non competitiva, quest'ultima pero' con diverse possibili varianti. 11. Inibizione competitiva. L'inibitore competitivo in genere si combina con l'enzima a livello del sito attivo impedendo l'accesso del substrato. A causa di questa modalita' di combinazione il substrato e l'inibitore sono mutuamente esclusivi e non si puo' formare il complesso ternario enizma-inibitore-substrato. Lo schema di reazione e':  Se la concentrazione di substrato viene aumentata molto fortemente, idealmente fino a tendere ad infinito, i termini che non contengono [S] diventano trascurabili e la Vmax risulta uguale a [Etot] k3, identica a quella che si puo' misurare in assenza dell'inibitore; pertanto l'inibitore competitivo aumenta il valore di KM e lascia invariato quello di Vmax. Questa proprieta' dell'inibitore competitivo e' molto importante dal punto di vista fisiologico perche' quando e' presente l'inibitore il substrato si accumula e alla fine sposta l'inibitore dal sito attivo e rimuove l'inibizione: il sistema risulta protetto dall'avvelenamento che l'inibitore potrebbe causare (l'inibizione competitiva e' un caso di identical linkage). I grafici di Michaelis e di Lineweaver per un caso di inibizione competitiva sono i seguenti:  12. Inibizione non competitiva pura. Nell'inibizione non competitiva, l'inibitore si lega ad un sito diverso dal sito attivo e si puo' formare il complesso ternario EIS. Se l'inibizione non competitiva e' "pura" non c'e' linkage tra inibitore e substrato e l'enzima ha la stessa affinita' per l'inibitore in presenza ed in assenza del substrato.  [EI] = [E] [I] / KI [EIS] = [E] [I] [S] / KM KI [Etot] = [E] (1 + [S]/KM + [I]/KI + [S][I]/KMKI)  13. Inibizione incompetitiva. L'inibizione incompetitiva o non competitiva e' un caso di heterotropic linkage. Lo schema di reazione e' il seguente:  [EI] = [E] [I] / KI [EIS] = [E] [S] [I] / KM KI' [Etot] = [E] (1 + [S]/KM + [I]/KI + [S][I]/KM KI') = = [E](KMKIKI' + [S]KIKI' + [I]KMKI' + [S][I]KI) / (KMKIKI' ) = [Etot][S]KIKI'k3 / ([S]KI([I] + KI') + (KMKI'([I] + KI))  se KI' < KI il legame del substrato favorisce l'inibitore e viceversa, quindi la KM apparente in presenza dell'inibitore sara' minore della KM misurata in assenza dell'inibitore; se KI' > KI il legame del substrato riduce l'affinita' dell'inibitore l'inibitore e viceversa, quindi la KM apparente in presenza dell'inibitore sara' maggiore della KM misurata in assenza dell'inibitore. |