1) La coagulazione e' il processo nel quale un danno vascolare viene temporaneamente riparato dapprima da un "tappo" piastrinico e poi da una rete formata dalla proteina fibrina. In questa lezione si discutono le basi biochimiche della seconda fase della coagulazione, l'attivazione della fibrina.
2) Struttura della fibrina e del fibrinogeno. a fibrina e' presente nel sangue sotto forma di fibrinogeno, il suo precursore inattivo prodotto dal fegato. Le strutture del fibrinogeno e della fibrina sono discusse in dettaglio in questo articolo.
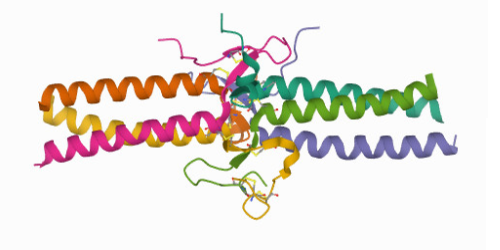
La fibrina e' una grande glicoproteina fibrosa (MW=340 kDa) formata da 6 subunita' uguali a due a due e denominate α, β ed γ. La struttura della fibrina e' pertanto α2β2 γ2. Sulla superficie delle subunita' della fibrina sono presenti aree idrofobiche specifiche che permettono il riconoscimento reciproco delle molecole di fibrina e la loro adesione (inizialmente non covalente).
E' necessario per la fisiologia del processo della coagulazione che la fibrina sia sempre presente nel sangue perche' il processo della coagulazione non puo' essere ritardato dalla necessita' di sintetizzare la proteina ex novo; per ottenere questo pero' e' necessario che la firbina sia presente nel sangue in una forma incapace di coagulare, che possa essere rapidamente convertita nella forma capace di coagulare. Per questa ragione, la fibrina viene sintetizzata dal fegato sotto forma del suo precursore inattivo, il fibrinogeno. Le catene polipeptidiche α e β del fibrinogeno sono piu' lunghe di quelle della fibrina perche' presentano delle estensioni all'estremita' carbossi-terminale, chiamate fibrinopeptidi A e B. La struttura del fibrinogeno risulta quindi Aα2Bβ2 γ2. I fibrinopeptidi si ripiegano sul corpo della macromolecola e coprono le aree di contatto necessarie alla polimerizzazione della fibrina.
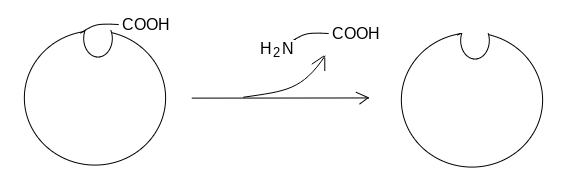
La conversione del fibrinogeno in fibrina richiede un evento di proteolisi specifica che idrolizzi il legame peptidico a livello dei fibrino peptidi; la proteasi che opera questa modifcazione del fibrinogeno e' la trombina.
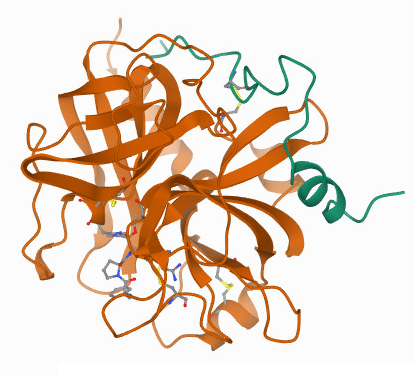
3) La trombina e' una proteasi a serina, lontanamente correlata alla tripsina, che digerisce selettivamente il legame peptidico dei fibrinopeptidi. Ovviamente e' presente nel sangue in forma inattiva, la protrombina, per le stesse ragioni fisiologiche ed evoluzionistiche per le quali anche la fibrina e' presente nella forma inattiva del fibrinogeno. Anche la modalita' con la quale la protrombina e' resa inattiva ed e' attivabile e' simile a quella della fibrina/fibrinogeno: la protrombina possiede una coda C-terminale che si ripiega sul sito attivo, coprendolo e rendendolo inaccessibile al substrato. La rimozione di questa coda C-terminale in un evento di proteolisi specifica libera il sito attivo e rende funzionale la trombina. Ci sono vari enzimi della coagulazione che sono in grado di attivare la trombina: la trombina stessa e i fattori della coagulazione VII e V.
4) La casacata proteolitica. Il meccanismo di attivazione della trombina richiede l'attivazione di una serie di enzimi proteolitici tutti molto specifici e molto simili alla trombina stessa, in quanto sintetizzati dal fegato sotto forma di precursori inattivi. Anche il meccanismo di attivazione e' analogo a quello della protrombina/trombina: nella loro forma inattiva tutti hanno una coda C-terminale che copre il sito catalitico e che deve essere rimossa proteoliticamente.
Per descrivere la cascata di attivazione proteolitica del processo della coagulazione conviene invertire l'ordine seguito fino ad ora e iniziare la descrizione dai fattori che si trovano piu' a monte nel processo, a maggiore distanza dalla trombina. Questo ci permette di osservare che esistono in effetti due vie di attivazione della protrombina, definite estrinseca e intrinseca, come nella figura qui sotto.
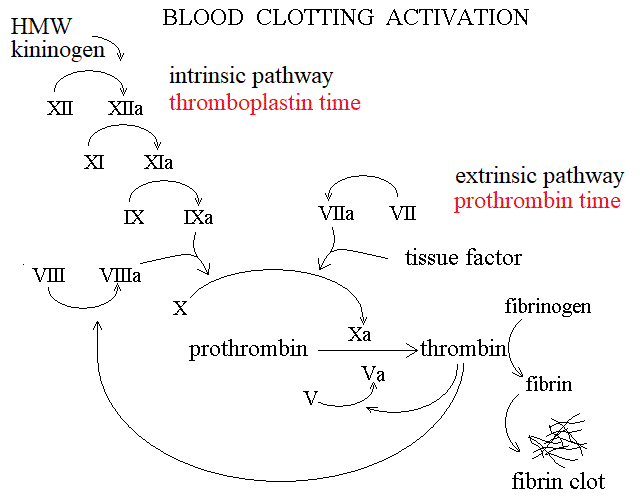
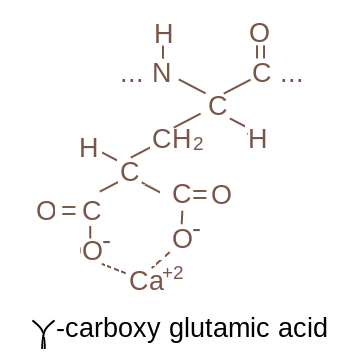
5) I fattori della coagulazione presentano alcune peculiarita' importanti. Vengono prodotti (dal fegato) e richiedono modificazioni post-traduzionali, consistenti nella γ-carbossilazione di alcuni residui superficiali di acido glutamico. La reazione enzimatica di γ-carbossilazione richiede come cofattore la vitamina K. In mancanza della modificazione post-traduzionale sono inattivi. L'acido γ-carbossi-glutamico e' un sito di legame per lo ione calcio che e' richiesto per la loro attivita' catalitica. I chelanti del calcio sono infatti utilizzati in vitro come anticoagulanti (ma non possono essere usati a questo scopo in vivo).
6)I geni che codificano per i fattori della coagulazione sono tutti localizzati sul cromosoma X; di conseguenza i difetti ereditari della coagulazione seguono un modello di eredita' legata al sesso, nel quale i maschi sono malati e le femmine sono portatrici; l'esempio classico e' dato dalle emofilie.